Борьба с Streptococcus suis – это битва, которую свиноводы, ветеринары и исследователи всего мира ведут уже долгое время. S. suis является важным заболеванием, приводящим к менингиту, сепсису и другим инвазивным патологиям, в основном, у поросят после отъема. Генетическое разнообразие S. suis значительно затрудняет его диагностирование и ведение эпизоотического надзора. Кроме того, S. suis является так же и новейшим зоонозным заболеванием для работников, занятых в отрасли свиноводства (профессиональное заболевание). В некоторых регионах (особенно это заметно в некоторых странах Азии) эта болезнь стала часто приводить к серьезным вспышкам у персонала, имеющего контакт с заболевшими животными или зараженными свиными продуктами. Учитывая, что в настоящее время весь мир ограничивает применение антибиотиков, свиноводам придется больше полагаться на меры недопущения, чем на профилактическую/метафилактическую антибиотикотерапию. Итак, почему же на рынке нет эффективной вакцины против Streptococcus suis? (Segura M, 2015).

Все о Streptococcus suis
Streptococcus suis естественным образом присутствует в верхних дыхательных путях свиней, а так же в их желудочно-кишечном и половом трактах. Доля переносчиков этой бактерии в поголовьях свиней может доходить до 100%, какие-либо клинические симптомы при этом могут отсутствовать. Однако, бактерии от этих свиней-переносчиков может передаваться другим животным (Gottschalk M, Segura M., 2019).
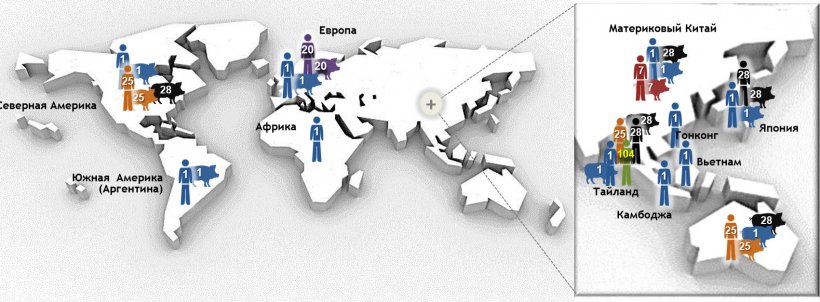
Рисунок 1. Самые важные типы последовательностей (STs) серотипа 2 Streptococcus suis, определенные мультилокусным секвенированием (MLST). Штаммы ST1 серотип 2 прочнее всего связаны с болезнью свиней и человека в Европе, Азии, Африке и Южной Америке (Аргентина). ST7, однолокусный вариант ST1, эндемичен в материковом Китае. Другая ситуация в Северной Америке, где описано всег несколько случаев инфекции ST1 у свиней и всего 1 случай – у человека. На самом деле, штаммы Североамериканского серотипа 2 относятся, в основном, к ST25 (человек и свиньи) и ST28 (только свиньи). Эта последняя ST так же ассоциируется с клиническими случаями у свиней в материковом Китае, Австралии, Японии и Тайланде. Интересно то, что Япония и Тайланд – единственные страны, из которых сообщали о случаях ST28 так же и у человека. Кроме того, случаи североамериканского ST25 были зафиксированы в Австралии и Тайланде. Наконец, ST20 превалентен только в Европе (в основном, в Нидерландах). На этом рисунке, числа (1, 20, 25, 28, 104) в разных местах представляют различные STs (т.е., ST1, ST20, ST25, ST28, ST104), и каждый ST показан различным цветом. Рисунок был взят, с изменениями, из: Segura M, Fittipaldi N, Calzas C, Gottschalk M. Critical Streptococcus suis virulence factors: Are they all really critical? Trends Microbiol. 2017; 25(7):585-599. doi: 10.1016/j.tim.2017.02.005, разрешение на использование имеется.
S. suis распространена во всем мире, но в разных регионах она может быть разной (Рис.1). Изначально эта бактерия была поделена на 35 серотипов - по сахарам, обнаруженным в «капсуле», окружающей наружную мембрану (в отношении нескольких из этих серотипов в настоящее время ведутся дебаты насчет того, относятся ли они S. suis). Чаще всего при клинических случаях у свиней обнаруживают серотипы: 2 (во всем мире); 9 (некоторые страны Европы); 3, ½ и 7 (в основном, Северная Америка, а серотип 3 – еще и в Азии). S. suis еще классифицируется по «секвенс-типам» (типам нуклеотидных последовательностей), в основе которых лежит «отпечаток пальцев» ДНК, так называемый, ДНК-фингерпринт (Goyette Desjardins, и др., 2014). Поэтому, каждый серотип содержит многочисленные секвенс-типы (Рис.1). Все это разнообразие означает, что каждая отдельная S. suis-инфекция обладает уникальными характеристиками в плане серотипа, секвенс-типа, зоонозного потенциала и клинических последствий. Такое огромное количество вариаций объясняет, почему так трудно создать одну «универсальную» вакцину, которая по всему миру защищала бы свиней от всех S. suis-инфекций (Goyette Desjardins, и др., 2014).
Типы вакцин
Существует большое число типов вакцин, все они обладают своими достоинствами и недостатками. Животных можно защитить, вводя им либо компонент (субъединицу) этой бактерии или живую аттенуированную бактерию, либо «убитую» (инактивированную) бактерию. Экспериментальные субъединичные вакцины выглядят обещающе, однако, требуют сильных стимуляторов-адьювантов (растворов, усиливающих реакцию иммунной системы). Кроме того, поскольку S. suis так разнообразна, подобрать специфический компонент (ранее – белок), способный защитить от всех штаммов S. suis, остается проблематичным. Комбинирование различных белков S. suis (антигенов) в субъединичной вакцине являлось бы, скорее всего, наилучшим шансом на обеспечение более «универсальной» и эффективной защиты. С другой стороны, при том гипотетическом преимуществе, что имеющиеся живые аттенуированные вакцины не требуют никаких бустеров или адьювантов, они представляют риск для здоровья человека, учитывая, что S. suis – это зоонозное заболевание и введенный штамм может «вспомнить» о вирулентности. Второй недостаток живых аттенуированных вакцин против S. suis – это то, что натурально или экспериментально зараженные животные продуцируют мало антител, поэтому трудно предугадать, сможет ли аттенуированный штамм (который вполне может элиминироваться хозяином) индуцировать защитную реакцию, когда вирулентный штамм этого сделать не смог. Следует отметить, что как раз этим фактом можно было бы объяснить, почему в большинстве исследований, связанных с живыми аттенуированными вакцинами, прибегали к схеме с многократными инъекциями (Segura M., 2015).
Последним типом вакцин, широко применяемым для профилактики S. suis, являются «убитые» (инактивированные) бактерии или «бактерины», которые снижают риск для здоровья человека, но их способность стимулировать иммунную систему так же ограничена, поэтому результаты их применения противоречивы (Segura M, 2015). На самом деле, аутогенные бактерины представляют собой единственный доступный «в полях» вариант. Такие вакцины – это бактерины, приготовленные под конкретную ферму путем забора проб у зараженных животных. Вследствие этого, несмотря на гигантское разнообразие S. suis-инфекций, привитые животные оказываются защищенными от того же штамма(ов), что вызвал клинические проблемы в данном конкретном поголовье. Однако, диагностика S. suis в качестве основной причины заболевания может осложнить выбор штамма(ов) для включения в аутогенную вакцину. Тем не менее, прежде чем делать какие-то выводы, на которых будут основаны окончательные решения, необходимо провести дополнительные исследования всех типов вакцин. По состоянию на 2019 г. в подавляющем большинстве публикаций на тему иммунизации от S. suis посвящены изучению субъединичных вакцин, затем – бактеринов, и, наконец - живых аттенуированных (ослабленных) вакцин (Рис.2).
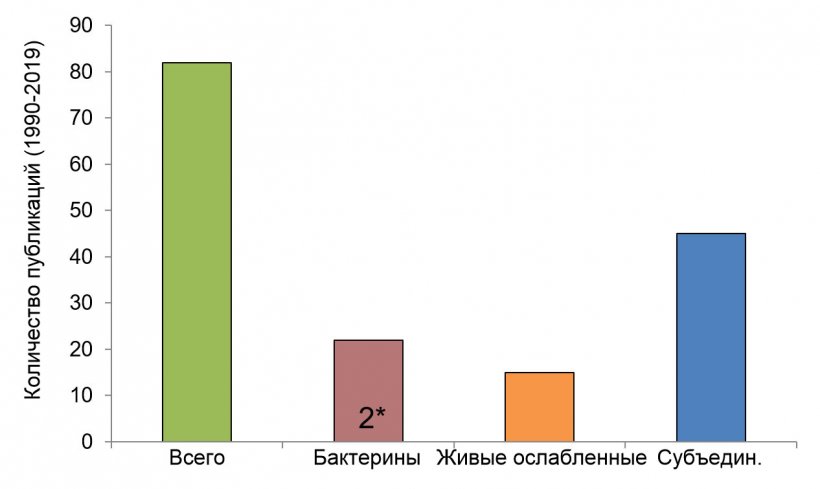
Рисунок 2. Количество исследований по типу вакцины от Streptococcus suis, начиная с 1990 г. (с использованием информации из «Segura M, 2015» и базы данных PubMed). В некоторых работах бактериновые вакцины не являлись предметом прямого исследования, но изучались в форме контроля. 2* Опубликовано всего два исследования, в которых использовались аутогенные бактерины, приготовленные лицензированными компаниями.
Проблемы при разработке вакцин от S. suis
До сей поры отсутствуют какие-либо международные соглашения о том, как должна тестироваться действенность вакцин, а это означает, что сравнивать результаты действия различных формул весьма затруднительно. Заметно отличаются друг от друга как сами исследования – формулы вакцин, бустеры и прививаемые животные (свиноматки vs поросята), так и шаги, предпринимаемые для того, чтобы определить, защищает ли вакцина животного! Классифицируя антитела по какому-либо изотипу (или подклассу антител) важно иметь возможность предсказывать тип иммунного ответа, генерируемого иммунизацией: идеальный ответ вызывает распад бактерий. В случае с S. suis этот эффект может быть измерен, прибегнув к киллинг-анализу, который подтвердит, что продуцированные вакциной антитела являются функционирующими. Функциональные свойства зависит от изотипа продуцированного антитела: не все они способны вызвать элиминацию S. suis. Однако, в настоящее время не существует стандартизированного протокола для тестирования действенности вакцины от S. suis (как то: модельное животное, искусственное инфицирование, киллинг-анализы и т.п.), что вносит еще больше сумятицы в интерпретацию результатов тестирования вакцин (Segara M, 2015). Например, из 17 исследований вакцин против S. suis, опубликованных в промежуток 2015 – 2019 г.г., большинство проводило анализ на присутствие антител и проверку смертности на мышах. Менее половины вышеупомянутых исследований проводили киллинг-анализ (при этом значительно различалась методология) и/или анализирование типа/ов продуцированных антител. Еще меньше было тех, кто провел тесты по оценке заражаемости/смертности на свиньях! Обратить внимание!: если вакцинирование мышей дает веские основания ожидать отрицательный результат, обещающие варианты вакцин абсолютно обязательно должны тестироваться на свиньях, причем в условиях контролируемого экспериментального заражения (Рис.3). До сих пор, экспериментальное инфицирование S. suis поросят в лабораторных условиях дает неустойчивые результаты, что еще больше затягивает разработку вакцин. Действительно, большинство серотипов S. suis неспособны вызвать каких-либо клинических проявлений в экспериментальных условиях. Что касается аутогенных вакцин, отчетов крайне мало (всего две опубликованные статьи за последние 30 лет, Рис.2) или они неполные, к тому же в большинстве из них отсутствует контрольная (неинфицированная) группа, что не позволяет сделать каких-то научно обоснованных выводов (Segura M, 2015).
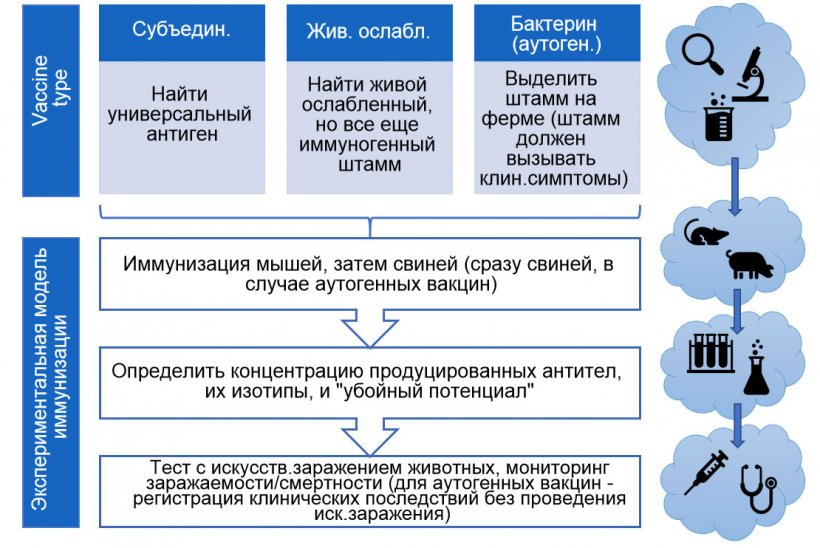
Рисунок 3. Шаги по экспериментальному тестированию действенности вакцин (по типам вакцин)

К несчастью, само по себе тестирование вакцин – это не единственная область, где нам не хватает знаний. Необходимо дополнительно изучать влияние материнских антител, чтобы можно было окончательно определить, что предпочтительнее – вакцинировать свиноматок или поросят? И когда? Это ключ к поиску оптимального окна для вакцинации поросенка: после того, как переданные свиноматкой антитела уже исчезли, но до того, как поросенок оказался полностью незащищенным (и, таким образом, уязвимым перед инфекцией). Наконец, подобранная вакцина должна быть, также, практичной для масштабного применения: количество необходимых бустеров должно быть сведено к минимуму, приоритетным должна быть вакцинация свиноматок, а не поросят – все это может оказаться полезным производителям в плане снижения денежных и трудозатрат. Все это еще больше осложняет создание идеальной вакцины.
Что нужно
С ростом ограничений на использование антибиотиков во всем мире, решающее значение имеет проведение большего числа исследований по разработке и/или улучшению вакцин против S. suis. Учитывая огромное разнообразий инфекций S. suis по регионам, аутогенные инфекции, вероятно, будут лучшим вариантом для защиты от этой бактерии, представляющей огромный риск для здоровья и свиней, и человека. Тем не менее, протокол испытаний для этих вакцин требует стандартизации на международном уровне, и необходимо провести дополнительные исследования, чтобы быстро сделать согласованные выводы по этому вопросу, прежде чем мы потеряем контроль над S. suis.



